
esCCO
Переопределите качество ухода с esCCO
Nihon Kohden переопределяет качество ухода с помощью инновационной технологии—esCCO (оценочный непрерывный сердечный выброс), вводя объемную информацию на всех уровнях ухода, несмотря на уровень инвазивности. esCCO — это новая технология для определения сердечного выброса с использованием времени прохождения пульсовой волны (PWTT), полученного из сигналов пульсоксиметрии и ЭКГ. Производительность esCCO для отслеживания изменений сердечного выброса и ударного объема была оценена в клинических исследованиях, и его точность была признана актуальной для клинического использования. Поскольку esCCO рассчитывает сердечный выброс с использованием стандартных параметров измерения, он не требует специальных техник или специальных расходных материалов. С esCCO возможно обеспечить оптимальное гемодинамическое управление пациентами, которые не могли быть измерены с помощью сердечного выброса из-за стоимости или нехватки человеческих ресурсов.
Надежная тенденция производительности
Легко
Без дополнительных датчиков
esCCO для оптимизации жидкости
Сообщается, что оптимальное управление жидкостями на основе объемных параметров, таких как ударный объем и сердечный индекс, может улучшить результаты лечения пациентов, включая сокращение продолжительности пребывания и снижение уровня осложнений. Поэтому сейчас растет спрос на менее инвазивные и более эффективные методы управления гемодинамическими тенденциями для улучшения ухода за пациентами. Неинвазивный и простой в использовании esCCO может предоставить полезное решение для этой цели, компенсируя недостатки других методов, доступных в настоящее время на рынке.
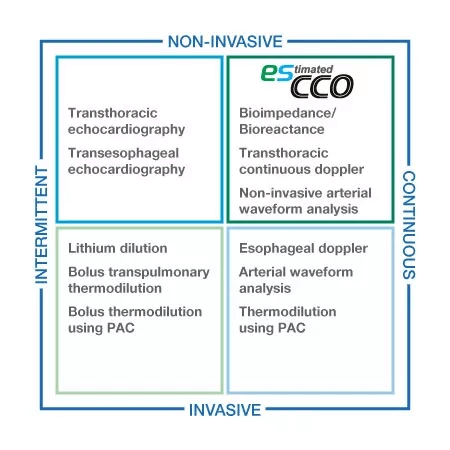
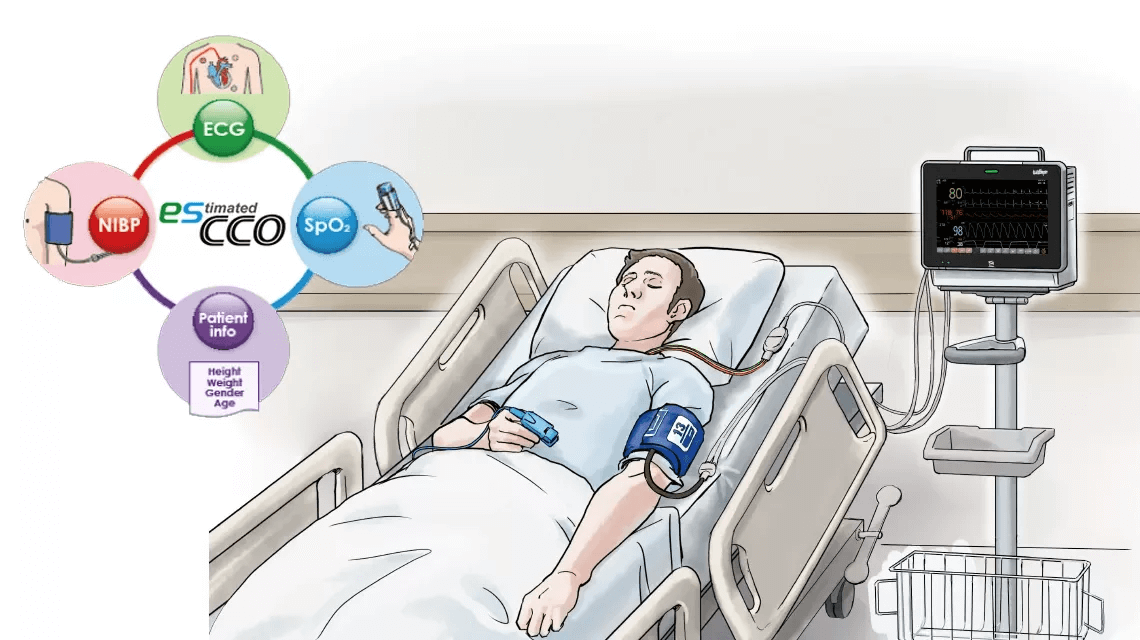
Объемная информация для всех уровней ухода
esCCO предоставляет информацию о сердечном выбросе, используя только общие параметры жизненно важных показателей, такие как ЭКГ, SpO2 и артериальное давление, не требуя дополнительных датчиков или специального обучения. Мониторинг гемодинамических тенденций будет доступен с esCCO для всех уровней ухода, не только во время крупных операций, но и при менее рискованных процедурах для пациентов с высоким риском, у которых наблюдается повышенная вероятность кровотечения или любого гемодинамического стресса. Кроме того, esCCO может быть надежным показателем при введении жидкости в различных клинических условиях. Добавление esCCO к традиционному мониторингу пациентов может привести к оптимизации управления жидкостями, снижению риска осложнений и, в конечном итоге, к лучшим результатам, включая сокращение продолжительности пребывания.
Потенциальные применения esCCO
Гемодинамический мониторинг после удаления катетера легочной артерии или транспульмональной термодилюции.
Гемодинамическая оптимизация пациентов, не подходящих для более агрессивных и рискованных методов (например, катетер легочной артерии).
Поддержка в процессе принятия решений для целенаправленного управления жидкостями и не только.
Инструмент сортировки для раннего выявления внезапного ухудшения состояния.
1 Ishihara H, Okawa H, Tanabe K, Tsubo T, Sugo Y, Akiyama T, Takeda S. A New Non-Invasive Continuous Cardiac Output Trend Solely Utilizing Routine Cardiovascular Monitors. J Clin Monit Comput 2004; 18: 313–320.
2 Yamada T, Tsutsui M, Sugo Y, Sato T, Akazawa T, Sato N, Yamashita K, Ishihara H, Takeda J. Multicenter Study Verifying a Method of Noninvasive Continuous Cardiac Output Measurement Using Pulse Wave Transit Time: A Comparison with Intermittent Bolus Thermodilution Cardiac Output. Anesth Analg. 2012 Mar 30
3 Wakeling HG et al. Intraoperative oesophageal Doppler guided fluid management shortens postoperative hospital stay after major bowel surgery. Br J Anaesth 2005; 95 : 634-42.
4 Mayer J et al. Goal-directed intraoperative therapy based on autocalibrated arterial pressure waveform analysis reduces hospital stay in high-risk surgical patients: a randomized, controlled trial. Crit Care 2010; 14: R18.
Принцип esCCO
Время Прохождения Пульсовой Волны как Важная Технология для esCCO
Время прохождения пульсовой волны (PWTT) определяется как время от пика R-волны на ЭКГ до точки подъема пульсовой волны. Точка подъема пульсовой волны определяется как точка, в которой дифференцированная пульсовая волна достигает 30% от своей максимальной амплитуды. PWTT состоит из трех интервалов: периода предвыброса (PEP), времени прохождения пульсовой волны через эластичную артерию (T1) и времени прохождения пульсовой волны через периферические артерии (T2) (Рисунок 1).
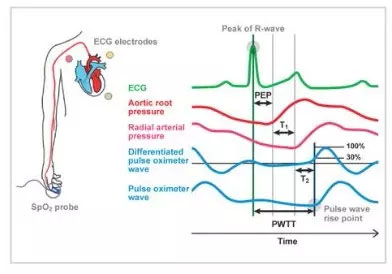
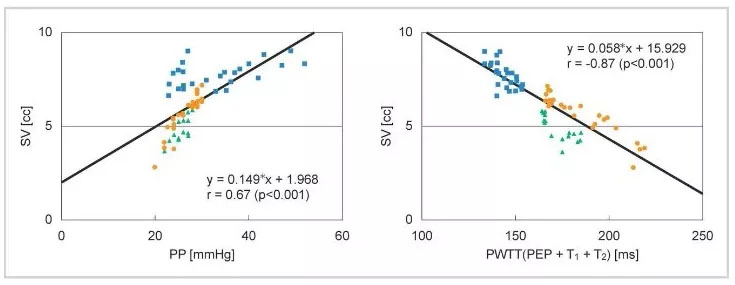
PEP отражает сократимость сердца и преднагрузку и сокращается по мере увеличения сократимости сердца и преднагрузки. T1 зависит от эластичности артерий и сокращается при повышении артериального давления. T2 отражает сосудистое сопротивление по мере расширения кровеносного сосуда. Таким образом, основываясь на различных элементах гемодинамического управления, включенных в PWTT, в сочетании с физиологическими данными, связанными с сердечным выбросом (CO), мы проверяли его клиническое применение. В результате была предпринята первоначальная попытка вывести артериальное давление из PWTT. Однако стало ясно, что изменения в PWTT были различными при введении сердечно-сосудистых агонистов. Было замечено, что PWTT и ударный объем (SV) показывают хорошую корреляцию, даже когда изменения артериального давления и SV не совпадают при введении лекарств (Рисунок 2).
Формула esCCO
Большинство существующих устройств для измерения сердечного выброса используют метод контуров пульса, который рассчитывает объем по волне артериального давления, как принцип измерения. Это показывает, что существует хорошая корреляция между ударным объемом (SV) и пульсовым давлением (PP) (Уравнение (1)).
SV = K × PP (1) K: постоянная
Также, в базовой концепции esCCO, PWTT и SV на Рисунке 2 находятся в хорошей корреляции, что можно показать как уравнение (2).
SV = α’ × PWTT + β’ (2) α’: постоянная β’: коэффициент
Уравнение (2) можно расширить до уравнения (3), используя уравнение (1) для включения компонента эластичности K.
SV= K × ( α × PWTT + β ) (3) α: постоянная, β и K: коэффициенты
На основе вышеизложенного, сердечный выброс непрерывно измеряется с использованием PWTT, и esCCO получается с использованием уравнения (4).
CO = SV × HR = K × (α × PWTT + β) × HR = esCCO (4)
α: постоянная, β и K: коэффициенты
Калибровка esCCO
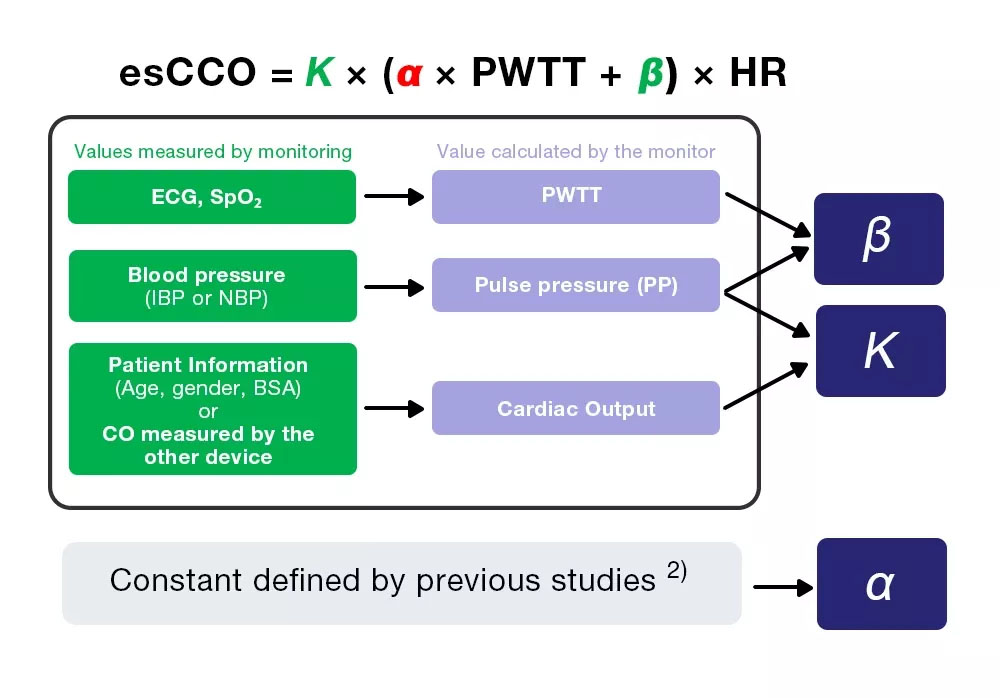
esCCO получает сердечный выброс из уравнения (4), которое включает три коэффициента (K, α и β).
esCCO = K × (α ×PWTT +β) ×HR (4)
Из трех коэффициентов α является постоянной (2), полученной из предыдущих исследований. K и β определяются путем ввода трех значений (PWTT, PP и CO), рассчитанных путем мониторинга во время калибровки. Однако CO для калибровки получается из информации о пациенте, что позволяет проводить неинвазивное измерение, что является одной из главных особенностей esCCO.
Ссылка
1) Sugo Y, UkawaT, Takeda S, Ishihara H, Kazama T, Takeda Z. 2010. A Novel ContinuousCardiac Output Monitor Based on Pulse Wave Transit Time. Conf Proc IEEE Eng MedBiol Soc. 2010: 2853-6.
2) Ishihara H, Okawa H, Tanabe K, Tsubo T, Sugo Y, Akiyama T, Takeda S. A New Non-Invasive Continuous Cardiac Output Trend Solely Utilizing Routine Cardiovascular Monitors. J Clin Monit, 2004; 18: 313–320.
Эффективность, основанная на доказательствах
В 2004 году мы сообщили, что esCCO имеет высокую корреляцию с непрерывным сердечным выбросом (CCO). Проводя несколько клинических испытаний, был составлен следующий отчет о точности и отзывчивости, которые являются ключевыми моментами производительности измерений.
Точность измерения
В 2009 году эффективность esCCO в практическом применении была оценена в многоцентровом исследовании в 7 учреждениях Японии, и результаты исследования были опубликованы в статье в 2012 году.
Многоцентровое исследование, проверяющее метод неинвазивного непрерывного измерения сердечного выброса с использованием времени прохождения пульсовой волны: сравнение с сердечным выбросом при интермиттирующей болюсной термодилюции
Авторы:Yamada T, Tsutsui M, Sugo Y, Sato T, Akazawa T, Sato N, Yamashita K, Ishihara H, Takeda J. Ссылка:Anesth Analg 2012;115:82-6. July 2012, Vol.115, No.1.
Предыстория
Многие технологии были разработаны для менее инвазивного мониторинга сердечного выброса. esCCO является одной из технологий, определяющих сердечный выброс с использованием времени прохождения пульсовой волны (PWTT). При использовании вместе с базовым мониторингом ЭКГ, SpO2 и артериального давления с использованием электродов ЭКГ, датчиков SpO2 и манжет, esCCO может быть применим для клинического мониторинга кровообращения у всех пациентов, включая пациентов с низким риском. Эффективность esCCO была оценена с использованием PWTT в многоинституциональном совместном исследовании.
Метод
В исследовании сравнивались esCCO и сердечный выброс, измеренный методом интермиттирующей болюсной термодилюции (ICO), у 213 пациентов в 7 учреждениях Японии (139 случаев в отделении интенсивной терапии, 74 случая в операционной). У всех пациентов измеряли ЭКГ, SpO2 и инвазивное артериальное давление, и esCCO калибровали один раз. Для измерения ICO сердечный выброс измеряли один раз в день у пациентов в отделении интенсивной терапии и ежечасно у пациентов в операционной, а также непосредственно перед удалением катетера легочной артерии у пациентов обеих групп. ICO и esCCO сравнивались с помощью корреляционного анализа и анализа Бланда-Альтмана, также оценивались изменения смещения со временем.
Результат
Корреляция между esCCO и ICO
Всего было получено 587 точек измерения от 213 пациентов. Демографические данные пациентов представлены в Таблице 1.
n | Возраст | Пол (М/Ж) | Рост (см) | Вес (кг) | ПП (㎡) | |
|---|---|---|---|---|---|---|
| Всего | 213 | 65.1 ± 12.7 | 142/71 | 160.0 ±10.3 | 59.2 ±12.5 | 1.61 ±0.20 |
Таблица 1. Демографические данные пациентов
Корреляция между esCCO и ICO составила r = 0,79 (p<0,01), а смещение ± точность составили 0,13 ± 1,15 (л/мин), что свидетельствует о хорошей точности измерений esCCO, эквивалентной ICO (Рисунок 4)
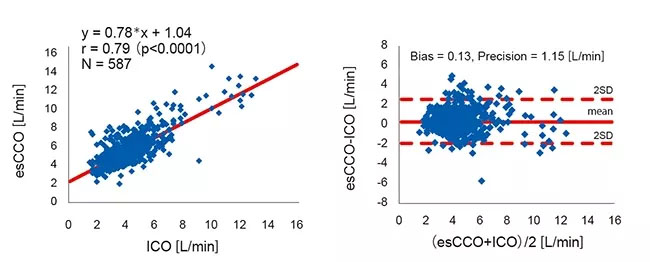
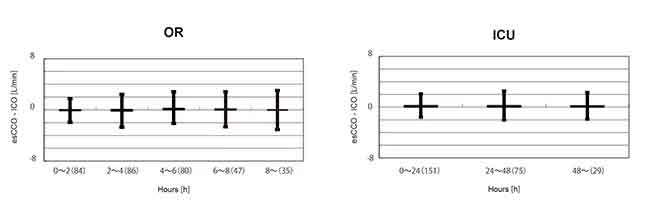
95% доверительный интервал для среднего смещения между esCCO и ICO составил от 0,04 до 0,22. Это было в пределах ±0,3 (л/мин), что считается приемлемым для клинического использования. Для оценки изменений смещения со временем данные за период после калибровки в группе OR были разделены на 5 интервалов по 2 часа каждый. Значительной разницы в смещении этих 5 интервалов не обнаружено. (ANOVA Уэлча p = 0,07) Также в группе ICU данные после калибровки были разделены на 3 интервала по 24 часа каждый. Значительной разницы в смещении этих 3 интервалов не обнаружено. (ANOVA для повторных измерений P = 0,781) (Рисунок 5).
Резюме
Была сильная корреляция между esCCO и ICO, и смещение было небольшим. Изменение смещения со временем также было небольшим.
Отзывчивость
В 2015 году был проведен сравнительный анализ с методом измерения, основанным на инвазивной волне артериального давления (APCO), который широко используется во многих учреждениях для измерения сердечного выброса. Сердечный выброс по методу интермиттирующей болюсной термодилюции (ICO) был использован в качестве основы для сравнения, и сравнение изменений во времени подтвердило, что отзывчивость была сопоставима с APCO.
Сравнение способности двух непрерывных мониторов сердечного выброса измерять тенденции сердечного выброса: оцененный непрерывный сердечный выброс, измеренный по модифицированному времени прохождения пульсовой волны, и устройство для измерения сердечного выброса на основе контуров артериального пульса
Авторы:Terada T, Oiwa A, Maemura Y, Robert S, Kessoku S, Ochiai R.Reference: J Clin Monit Comput. 2015 Sep 14.
Предыстория
Трансплантация почки связана с многочисленными сердечно-сосудистыми аномалиями, увеличивающими сердечный выброс и снижающими артериальное давление и сосудистое сопротивление. Поэтому периоперационный мониторинг этих параметров имеет решающее значение для пациентов с трансплантацией почки.
В этом исследовании сравнивались esCCO, сердечный выброс, измеренный методом интермиттирующей болюсной термодилюции (ICO), и сердечный выброс, основанный на артериальном давлении (APCO), который основан на наблюдении за волной артериального давления.
Метод
Взрослые пациенты, запланированные на пересадку почки и способные дать информированное согласие, были включены в оценку в Медицинском центре Университета Тохо Омори.
У всех пациентов измеряли ЭКГ, SpO2 и инвазивное артериальное давление.
ICO, esCCO и APCO измеряли в следующие 4 момента: после индукции анестезии, перед началом наложения швов на пересаженную почку, перед артериальным зажимом (артериальная реваскуляризация) и в конце операции.
Результаты для каждого алгоритма сравнивались с использованием корреляционного анализа, анализа Бланда и Альтмана и анализа полярного графика.
Результат
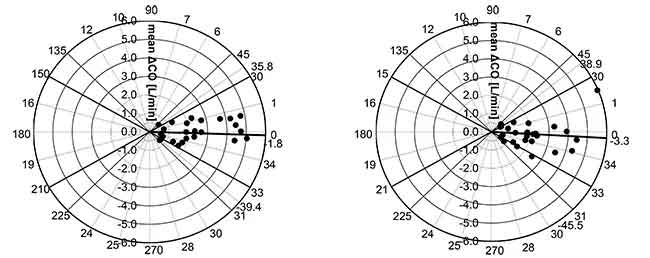
Средний угловой сдвиг esCCO и ICO составил -1,8°, радиальные пределы согласия составили ± 37,6°. (Рисунок 6. Слева)
Средний угловой сдвиг APCO и ICO составил -3,3°, радиальные пределы согласия составили ± 42,2°. (Рисунок 6. Справа)
Таким образом, можно сказать, что корреляция, смещение и способность к тренду между esCCO и ICO сопоставимы с таковыми между APCO и ICO.
Отчет о случае (Рисунок 7) показывает, что способность к тренду у esCCO сопоставима с APCO.
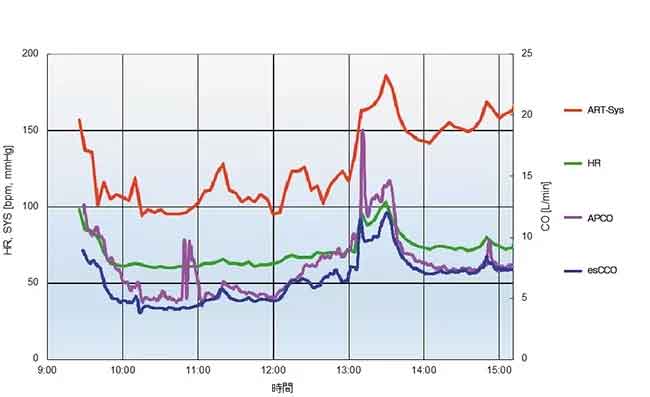
31-летний мужчина ростом 180 см и весом 93,8 кг. Измеренные значения APCO и esCCO составили соответственно 6,5 л/мин и 4,7 л/мин после индукции анестезии, 7,3 л/мин и 6,5 л/мин перед началом наложения швов на пересаженную почку, 14,3 л/мин и 12,0 л/мин перед зажимом артерии (артериальная реперфузия) после инфузионной нагрузки и 7,4 л/мин и 7,4 л/мин в конце операции.
Резюме
Способность к тренду у esCCO клинически приемлема и сопоставима с анализом волновой формы артериального давления.
Ссылка
1 Ishihara et al. 2004. A new non-invasive continuous cardiac output trend solely utilizing routine cardiovascular monitors. J Clin Monit, Dec, 18: 313-320.
2 Lawrence C. Siegel, Maeve M. Hennessy, Ronald G. Pearl. 1996. Delayed Time Response of the Continuous Cardiac Output Pulmonary Artery Catheter. Anesth Analg
Загрузки материалов - esCCO
-
Hemodynamic Management Using esCCO
-
Non-Invasive Hemodynamics Monitoring
-
Hemodynamics Graph for GDT
-
Hemodynamic Evaluation Using esCCO during Cesarean Section under Spinal Anesthesia
-
Improving the standard of non-invasive hemodynamic monitoring
-
Comparison of trend performance of esCCO and APCO in kidney transplantation
-
esCCO Performance Report
-
Experience with esCCOin Surgery in Elderly Patients
-
Continuous Cardiac Output from ECG and SpO2
-
Hemodynamic Management Using Estimated Cardiac Output (esCCO)
-
Anesthesia Management Using Estimated Continuous Cardiac Output (esCCO)
-
Can Estimated Continuous Cardiac Output Be Used in the Same Manner as Arterial Pressure-Based Cardiac Output
