
esCCO
Redefinir la calidad de la atención con esCCO
Nihon Kohden está redefiniendo la calidad de la atención con una tecnología innovadora—esCCO (gasto cardíaco continuo estimado), al introducir información volumétrica en todos los niveles de atención a pesar del nivel de invasividad. esCCO es una nueva tecnología para determinar el gasto cardíaco utilizando el tiempo de tránsito de la onda del pulso (PWTT), que se obtiene de las señales de oximetría de pulso y ECG. El rendimiento de esCCO para rastrear cambios en el gasto cardíaco y el volumen sistólico ha sido evaluado en estudios clínicos y su precisión ha demostrado ser relevante para el uso clínico. Debido a que esCCO calcula el gasto cardíaco utilizando parámetros de medición estándar, no requiere técnicas especiales ni consumibles especiales. Con esCCO, es posible proporcionar una gestión hemodinámica óptima a los pacientes que no podían ser medidos con gasto cardíaco debido a costos o escasez de recursos humanos.
Rendimiento de tendencia confiable
Fácil
Sin sensores adicionales
esCCO para la optimización de fluidos
Se ha informado que la gestión óptima de fluidos basada en parámetros volumétricos como el volumen sistólico y el índice cardíaco podría mejorar los resultados del paciente, incluyendo una estancia hospitalaria más corta y una tasa de complicaciones reducida. Por lo tanto, ahora hay una creciente demanda de métodos menos invasivos y más eficientes para gestionar las tendencias hemodinámicas para una mejor atención al paciente. El esCCO no invasivo y fácil de usar puede proporcionar una solución útil para este propósito al compensar las deficiencias de otros métodos actualmente disponibles en el mercado.
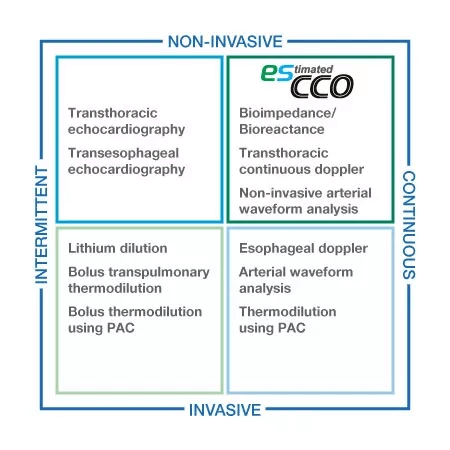
Información volumétrica para todos los niveles de atención
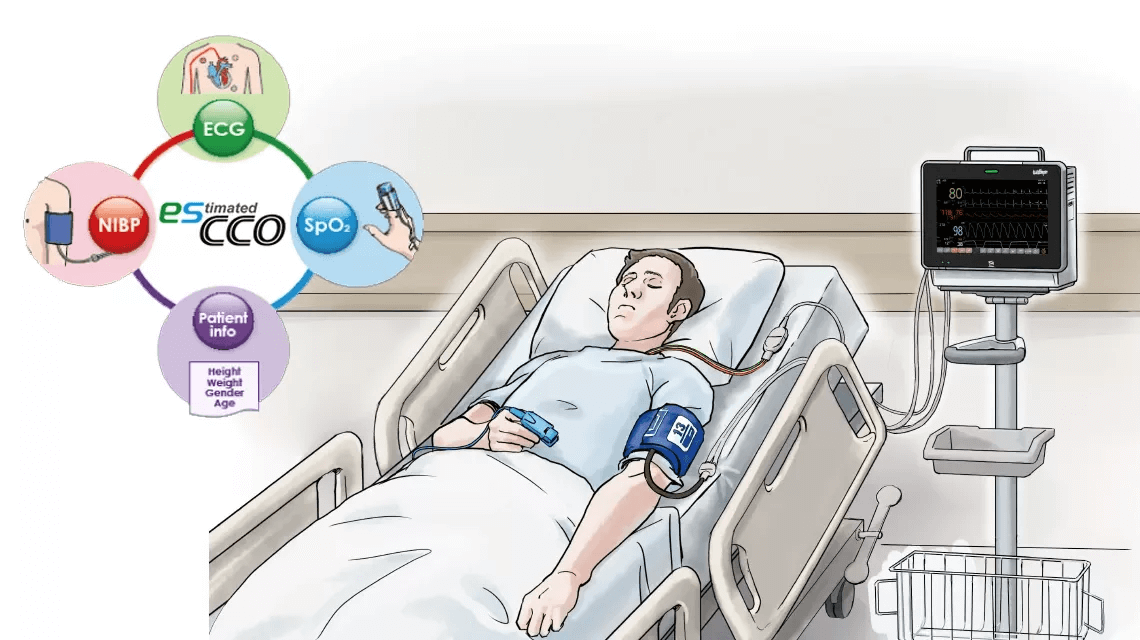
esCCO proporciona información sobre el gasto cardíaco utilizando solo parámetros comunes de signos vitales como ECG, SpO2 y presión arterial, sin necesidad de sensores adicionales ni entrenamientos especiales. La monitorización de tendencias hemodinámicas estará disponible con esCCO para todos los niveles de atención, no solo durante cirugías mayores, sino también en procedimientos de menor riesgo para pacientes de alto riesgo que muestren una mayor probabilidad de sangrado o cualquier estrés hemodinámico. Además, esCCO puede ser un índice confiable durante la administración de fluidos en diversos entornos clínicos. Agregar esCCO a la monitorización convencional del paciente puede llevar a la optimización del manejo de fluidos, la disminución del riesgo de complicaciones y, finalmente, a mejores resultados, incluida una reducción de la estancia hospitalaria.
Aplicaciones potenciales de esCCO
Monitoreo hemodinámico después de la extracción del catéter de la arteria pulmonar o de termodilución transpulmonar.
Optimización hemodinámica de pacientes que no son elegibles para técnicas más agresivas y arriesgadas (es decir, catéter de la arteria pulmonar).
Apoyo en el proceso de toma de decisiones para la gestión de líquidos dirigida a objetivos y más.
Herramienta de triaje para la detección temprana del deterioro repentino.
1 Ishihara H, Okawa H, Tanabe K, Tsubo T, Sugo Y, Akiyama T, Takeda S. A New Non-Invasive Continuous Cardiac Output Trend Solely Utilizing Routine Cardiovascular Monitors. J Clin Monit Comput 2004; 18: 313–320.
2 Yamada T, Tsutsui M, Sugo Y, Sato T, Akazawa T, Sato N, Yamashita K, Ishihara H, Takeda J. Multicenter Study Verifying a Method of Noninvasive Continuous Cardiac Output Measurement Using Pulse Wave Transit Time: A Comparison with Intermittent Bolus Thermodilution Cardiac Output. Anesth Analg. 2012 Mar 30
3 Wakeling HG et al. Intraoperative oesophageal Doppler guided fluid management shortens postoperative hospital stay after major bowel surgery. Br J Anaesth 2005; 95 : 634-42.
4 Mayer J et al. Goal-directed intraoperative therapy based on autocalibrated arterial pressure waveform analysis reduces hospital stay in high-risk surgical patients: a randomized, controlled trial. Crit Care 2010; 14: R18.
Principio de esCCO
Tiempo de Tránsito de Onda de Pulso como Tecnología Esencial para esCCO
El tiempo de tránsito de la onda del pulso (PWTT) se define como el tiempo desde el pico de la onda R del ECG hasta el punto de ascenso de la onda del pulso. El punto de ascenso de la onda del pulso se define como el punto donde la onda del pulso diferenciada alcanza el 30 % de su amplitud máxima. PWTT consta de tres intervalos: período de preeyección (PEP), tiempo de tránsito de la onda del pulso a través de la arteria elástica (T1) y tiempo de tránsito de la onda del pulso a través de las arterias periféricas (T2) (Figura 1).
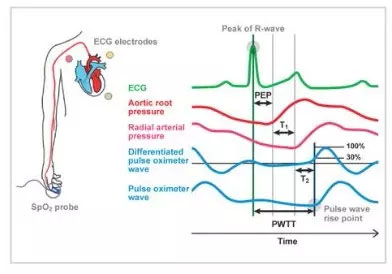
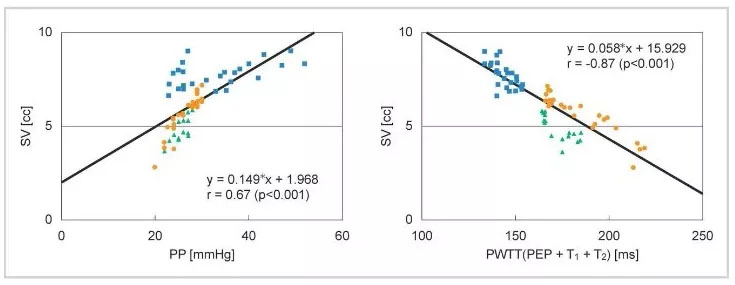
El PEP refleja la contractilidad cardíaca y la precarga y se acorta a medida que aumentan la contractilidad cardíaca y la precarga. T1 depende de la compliance arterial y se acorta cuando aumenta la presión arterial. T2 refleja la resistencia vascular a medida que el vaso sanguíneo se dilata. Por lo tanto, basándonos en los diversos elementos de la gestión hemodinámica incluidos en el PWTT, combinados con hallazgos fisiológicos relacionados con el gasto cardíaco (CO), hemos estado validando su aplicación clínica. Como resultado, se hizo un intento inicial de inferir la presión arterial a partir del PWTT. Sin embargo, quedó claro que los cambios en el PWTT eran diferentes cuando se administraban fármacos agonistas cardiovasculares. Se observó que el PWTT y el volumen sistólico (SV) muestran una buena correlación incluso cuando los cambios en la presión arterial y el SV no coinciden durante la administración de fármacos (Figura 2).
Fórmula de esCCO
La mayoría de los dispositivos existentes para la medición del gasto cardíaco utilizan el método de contorno de pulso, que calcula el volumen a partir de la forma de onda de la presión arterial, como principio de medición. Esto muestra que hay una buena correlación entre el volumen sistólico (SV) y la presión del pulso (PP) (Ecuación (1)).
SV = K × PP (1) K: una constante
También, en el concepto básico de esCCO, PWTT y SV en la Figura 2 están en buena correlación, lo que se puede mostrar como la ecuación (2).
SV= K × ( α × PWTT + β ) (3) α: una constante, β y K: coeficientes
La ecuación (2) se puede expandir a la ecuación (3) utilizando la ecuación (1) para incluir el componente de compliance K.
SV= K × ( α × PWTT + β ) (3) α: a constant, β and K: coefficients
Basado en lo anterior, el gasto cardíaco se mide continuamente utilizando PWTT, y esCCO se obtiene utilizando la ecuación (4).
CO = SV × HR = K × (α × PWTT + β) × HR = esCCO (4)
α: una constante, β y K: coeficientes
Calibración de esCCO
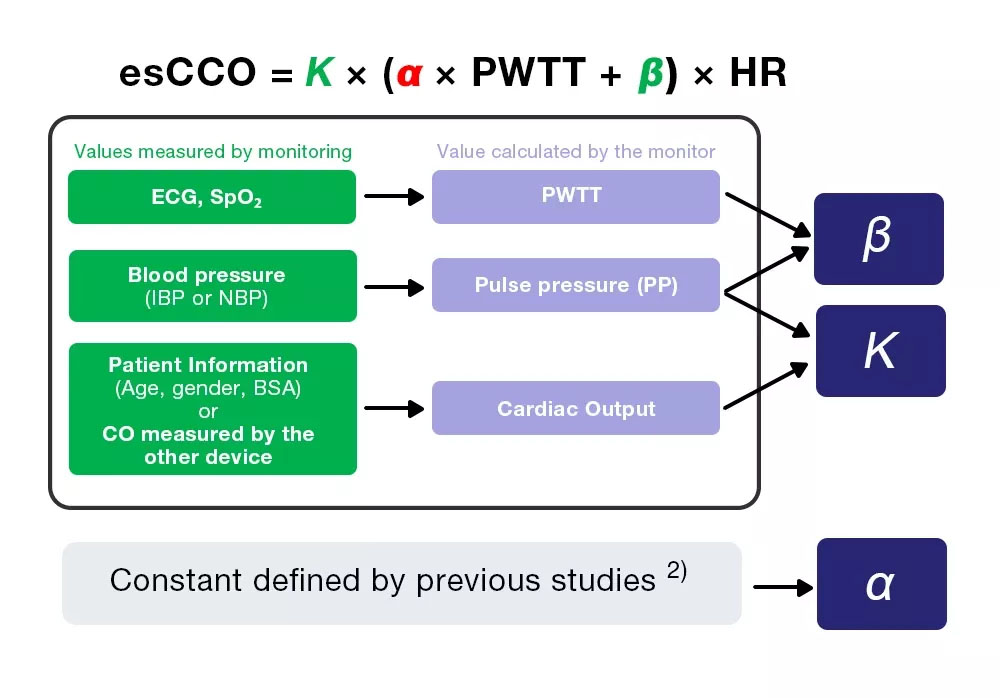
esCCO obtiene el gasto cardíaco de la ecuación (4), que incluye tres coeficientes (K, α y β).
esCCO = K × (α ×PWTT +β) ×HR (4)
De los tres coeficientes, α es una constante (2) que se obtiene de estudios previos. K y β se determinan ingresando los tres valores (PWTT, PP y CO) calculados mediante monitoreo durante la calibración. Sin embargo, el CO para la calibración se obtiene de la información del paciente, lo que permite una medición no invasiva, una de las mayores características de esCCO.
Referencia
1) Sugo Y, UkawaT, Takeda S, Ishihara H, Kazama T, Takeda Z. 2010. A Novel ContinuousCardiac Output Monitor Based on Pulse Wave Transit Time. Conf Proc IEEE Eng MedBiol Soc. 2010: 2853-6.
2) Ishihara H, Okawa H, Tanabe K, Tsubo T, Sugo Y, Akiyama T, Takeda S. A New Non-Invasive Continuous Cardiac Output Trend Solely Utilizing Routine Cardiovascular Monitors. J Clin Monit, 2004; 18: 313–320.
Rendimiento basado en evidencia
En 2004, informamos que esCCO tiene una alta correlación con el gasto cardíaco continuo (CCO). A medida que realizamos varias pruebas clínicas, se realizó el siguiente informe sobre precisión y capacidad de respuesta, que son los puntos clave del rendimiento de la medición.
Precisión de la medición
En 2009, la eficacia de esCCO en la aplicación práctica fue evaluada en un estudio multicéntrico en 7 instalaciones en Japón y los resultados del estudio fueron reportados en un artículo en 2012.
Estudio multicéntrico que verifica un método de medición continua no invasiva del gasto cardíaco utilizando el tiempo de tránsito de la onda de pulso: una comparación con el gasto cardíaco por termodilución en bolo intermitente
Autores:Yamada T, Tsutsui M, Sugo Y, Sato T, Akazawa T, Sato N, Yamashita K, Ishihara H, Takeda J. Referencia: Anesth Analg 2012;115:82-6. July 2012, Vol.115, No.1.
Antecedentes
Se han desarrollado muchas tecnologías para la monitorización del gasto cardíaco menos invasiva. esCCO es una de las tecnologías que determina el gasto cardíaco utilizando el tiempo de tránsito de la onda de pulso (PWTT). Cuando se utiliza junto con la monitorización básica de ECG, SpO2 y presión arterial utilizando electrodos de ECG, sondas de SpO2 y manguitos, esCCO puede ser aplicable para la monitorización circulatoria clínica de todos los pacientes, incluidos los pacientes de bajo riesgo. La eficacia de esCCO se evaluó utilizando PWTT en un estudio conjunto multi-institucional.
Método
El estudio comparó esCCO y el gasto cardíaco medido por termodilución en bolo intermitente (ICO) en 213 casos en 7 instalaciones en Japón (139 casos en UCI, 74 casos en quirófano). Se midieron ECG, SpO2 y presión arterial invasiva en todos los pacientes, y esCCO se calibró una vez. Para la medición de ICO, el gasto cardíaco se midió una vez al día para los pacientes de UCI y cada hora para los pacientes de quirófano, y justo antes de la extracción del catéter de la arteria pulmonar para ambos grupos de pacientes. ICO y esCCO se compararon mediante análisis de correlación y análisis de Bland-Altman, y también se evaluaron los cambios en el sesgo a lo largo del tiempo
Resultado
Correlación entre esCCO e ICO
Se obtuvieron un total de 587 puntos de medición de 213 pacientes. Las demografías de los pacientes se muestran en la Tabla 1.
n | Edad | Género (M/F) | Altura (cm) | Peso (kg) | SC (㎡) | |
|---|---|---|---|---|---|---|
| Total | 213 | 65.1 ± 12.7 | 142/71 | 160.0 ±10.3 | 59.2 ±12.5 | 1.61 ±0.20 |
Tabla 1. Demografía de los pacientes
La correlación entre esCCO e ICO fue r = 0,79 (p<0,01) y el sesgo ± precisión fue 0,13 ± 1,15 (L/min), lo que sugiere que esCCO tiene una buena precisión de medición equivalente a ICO (Figura 4).
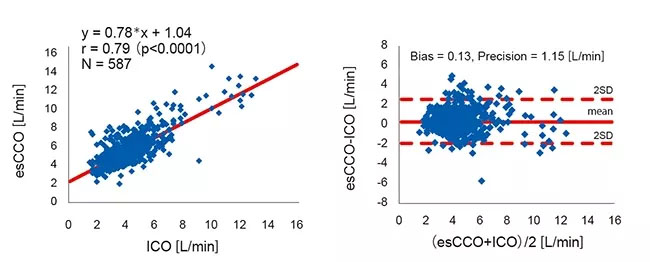
El intervalo de confianza del 95% para el sesgo medio entre esCCO e ICO fue de 0,04 a 0,22. Esto estaba dentro del rango de ±0,3 (L/min), lo cual se considera aceptable para uso clínico. Para evaluar los cambios en el sesgo a lo largo del tiempo, los datos para el período posterior a la calibración en el grupo OR se dividieron en 5 intervalos de 2 horas cada uno. No se encontró una diferencia significativa en el sesgo de estos 5 intervalos. (ANOVA de Welch p = 0,07) Además, en el grupo de UCI, los datos después de la calibración se dividieron en 3 intervalos de 24 horas cada uno. No se encontró una diferencia significativa en el sesgo de estos 3 intervalos. (ANOVA de medidas repetidas P = 0,781) (Figura 5).
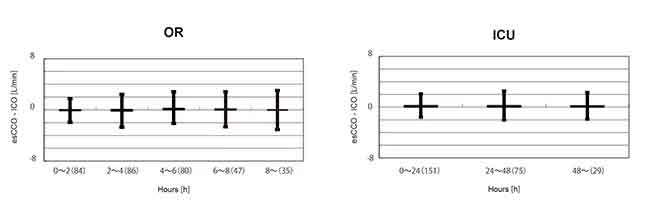
Resumen
Hubo una fuerte correlación entre esCCO e ICO y el sesgo fue pequeño. El cambio de sesgo a lo largo del tiempo también fue pequeño.
Capacidad de respuesta
En 2015 se informó de una comparación con un método de medición basado en la onda de presión arterial invasiva (APCO), que se utiliza ampliamente en muchas instalaciones para medir el gasto cardíaco. El gasto cardíaco por termodilución en bolo intermitente (ICO) se utilizó como base para la comparación y la comparación de los cambios a lo largo del tiempo confirmó que la capacidad de respuesta era comparable a la de APCO.
Comparación de la capacidad de dos monitores de gasto cardíaco continuo para medir las tendencias en el gasto cardíaco: gasto cardíaco continuo estimado medido por tiempo de tránsito de onda de pulso modificado y un dispositivo de gasto cardíaco basado en contorno de pulso arterial
Autores: Terada T, Oiwa A, Maemura Y, Robert S, Kessoku S, Ochiai R.Reference: J Clin Monit Comput. 2015 Sep 14.
Antecedentes
El trasplante de riñón está asociado con numerosas anomalías cardiovasculares, aumentando el gasto cardíaco y disminuyendo la presión arterial y la resistencia vascular. Por lo tanto, el monitoreo perioperatorio de estos parámetros es crucial para los pacientes de trasplante de riñón.
Este estudio comparó esCCO, el gasto cardíaco medido por termodilución en bolo intermitente (ICO) y el gasto cardíaco basado en la presión arterial (APCO), que se basa en la observación de la onda de presión arterial.
Método
Se inscribieron en la evaluación en el Centro Médico de la Universidad de Toho Omori a pacientes adultos programados para trasplante de riñón y capaces de proporcionar consentimiento informado.
Se midieron ECG, SpO2 y presión arterial invasiva en todos los pacientes.
ICO, esCCO y APCO se midieron en los siguientes 4 momentos: después de la inducción de la anestesia, antes de que comience la sutura del riñón trasplantado, antes del pinzamiento arterial (revascularización arterial) y al final de la cirugía.
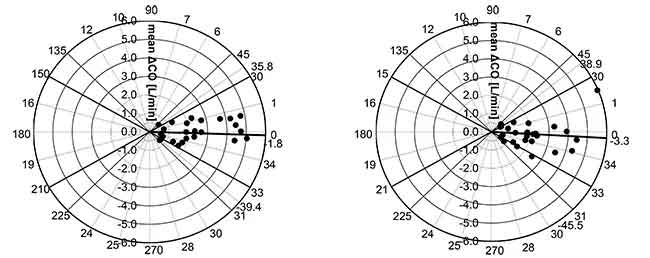
Los resultados de cada algoritmo se compararon mediante análisis de correlación, análisis de Bland y Altman y análisis de gráfico polar.
Resultado
El sesgo angular medio de esCCO e ICO fue de -1,8°, los límites radiales de acuerdo fueron de ± 37,6°. (Figura 6. Izquierda)
El sesgo angular medio de APCO e ICO fue de -3,3°, los límites radiales de acuerdo fueron de ± 42,2°. (Figura 6. Derecha)
Por lo tanto, podemos decir que la correlación, el sesgo y la capacidad de tendencia entre esCCO e ICO son comparables a los de APCO e ICO.
Un informe de caso (Figura 7) muestra que la capacidad de tendencia de esCCO es comparable con la de APCO.
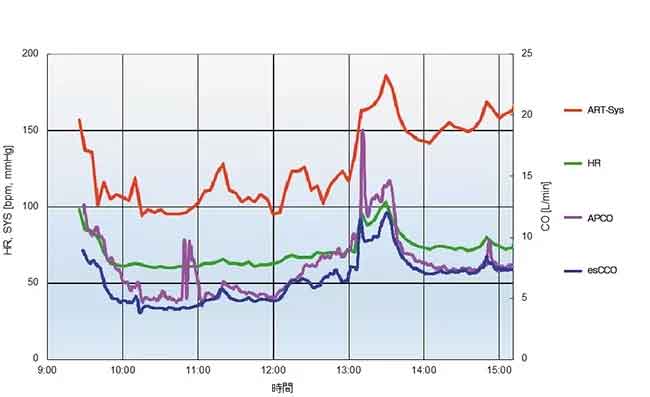
Hombre de 31 años con una altura de 180 cm y un peso de 93,8 kg. Los valores medidos de APCO y esCCO fueron, respectivamente, 6,5 L/min y 4,7 L/min después de la inducción de la anestesia, 7,3 L/min y 6,5 L/min antes del inicio de la sutura del riñón injertado, 14,3 L/min y 12,0 L/min antes del pinzamiento de la arteria (reperfusión arterial) después del desafío de fluidos, y 7,4 L/min y 7,4 L/min al final de la cirugía.
Resumen
La capacidad de tendencia de esCCO es clínicamente aceptable y comparable con el análisis de la forma de onda de la presión arterial.
Referencia
1 Ishihara et al. 2004. A new non-invasive continuous cardiac output trend solely utilizing routine cardiovascular monitors. J Clin Monit, Dec, 18: 313-320.
2 Lawrence C. Siegel, Maeve M. Hennessy, Ronald G. Pearl. 1996. Delayed Time Response of the Continuous Cardiac Output Pulmonary Artery Catheter. Anesth Analg
Descargas de material - esCCO
-
Hemodynamic Management Using esCCO
-
Non-Invasive Hemodynamics Monitoring
-
Hemodynamics Graph for GDT
-
Hemodynamic Evaluation Using esCCO during Cesarean Section under Spinal Anesthesia
-
Improving the standard of non-invasive hemodynamic monitoring
-
Comparison of trend performance of esCCO and APCO in kidney transplantation
-
esCCO Performance Report
-
Experience with esCCOin Surgery in Elderly Patients
-
Continuous Cardiac Output from ECG and SpO2
-
Hemodynamic Management Using Estimated Cardiac Output (esCCO)
-
Anesthesia Management Using Estimated Continuous Cardiac Output (esCCO)
-
Can Estimated Continuous Cardiac Output Be Used in the Same Manner as Arterial Pressure-Based Cardiac Output
